PRÁCTICA 13: LA PELOTA SALTARINA.
INTEGRANTES DEL EQUIPO
PIRY HERRERA JASSO
-3cpiryherreraj16.blogspot.mx
KEVIN EDUARDO JIMENEZ ROMO
-3ckevinjimenezr.blogspot.mx
LEGNA CAROLINA LIRA AGUILA
-3clegnaliraA18.blogspot.mx
BRISSA ARANDEY LOPEZ REYES
-3cbrissalopezr19blogspot.mx
KATIA DEYANIRA LOPEZ SERNA
-3cKatiaLopezs20.blogspot.mx
GUILLERMO AXEL MACIAS MACIAS
FECHA DE REALIZACION: 2 de Marzo de 2016
OBJETIVO:
Observar un cambio químico por medio de la elaboración de una pelota a partir de un polímero.
HIPOTESIS
-Suponíamos que hacer esta practica seria un procedimiento sencillo
-creímos que usando las cantidades indicadas en la practica obtendríamos una pelota bien hecha y con buenos resultados
INVESTIGACIÓN:
Qué es un polímero, usos del bórax.
POLIMERO
Polímero es una noción cuyo origen etimológico se encuentra en la lengua griega y se refiere a algo formado por diversos componentes. Y es que así lo certifica su origen etimológico. En concreto, deriva del griego, exactamente de la suma de dos elementos como son el prefijo “poli-”, que es equivalente a “muchos”, y el sustantivo “meros”, que puede traducirse como “partes”.
La acepción más habitual del término hace mención a un compuesto, ya sea sintético, natural o químico, que se crea a través de un fenómeno conocido como polimerización, a partir de la repetición de unidades estructurales.
Puede decirse que los polímeros son macromoléculasque se forman con la vinculación de otras clases demoléculas denominadas monómeros. La síntesis de los polímeros se produce por una reacción provocada por sus monómeros que se denomina, como ya mencionábamos, polimerización.
La polimerización puede desarrollarse como una reacción en cadena o a través de diversos pasos o etapas.
los polímeros naturales son aquellos que están presentes en la naturaleza. En este grupo es posible incluir al ADN, las proteínas y la quitina, entre otros. Los polímeros sintéticos, en cambio, se producen de forma industrial mediante la manipulación de los monómeros. El poliéster, el PVC y el nailon son ejemplos de polímeros sintéticos. polímero natural:algodón
polímero natural:algodón
BORAX
El bórax(Na2B4O7·10H2O,borato de sodio o tetraborato de sodio) es un compuesto importante del boro. Es el nombre comercial de la sal de boro. Es un cristal blanco y suave que se disuelve fácilmente enagua; con densidad (decahidrato) de 1.73 g/cm3. Si se deja reposar al aire libre, pierde lentamente su hidratación y se convierte en tincalconita (Na2B4O7 •5 H2O). El bórax comercial generalmente se deshidrata en parte.
USOS
pesticidas
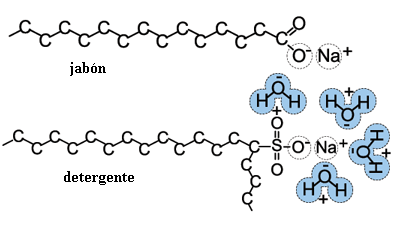
El bórax se utiliza ampliamente en detergentes, suavizantes, jabones, desinfectantes y pesticidas. Se utiliza en la fabricación de esmaltes, vidrio y cerámica. También se convierte fácilmente enácido bórico o en borato, que tienen muchos usos.
INTEGRANTES DEL EQUIPO
PIRY HERRERA JASSO
-3cpiryherreraj16.blogspot.mx
KEVIN EDUARDO JIMENEZ ROMO
-3ckevinjimenezr.blogspot.mx
LEGNA CAROLINA LIRA AGUILA
-3clegnaliraA18.blogspot.mx
BRISSA ARANDEY LOPEZ REYES
-3cbrissalopezr19blogspot.mx
KATIA DEYANIRA LOPEZ SERNA
-3cKatiaLopezs20.blogspot.mx
GUILLERMO AXEL MACIAS MACIAS
FECHA DE REALIZACION: 2 de Marzo de 2016
OBJETIVO:
Observar un cambio químico por medio de la elaboración de una pelota a partir de un polímero.
HIPOTESIS
-Suponíamos que hacer esta practica seria un procedimiento sencillo
-creímos que usando las cantidades indicadas en la practica obtendríamos una pelota bien hecha y con buenos resultados
INVESTIGACIÓN:
Qué es un polímero, usos del bórax.
POLIMERO
Polímero es una noción cuyo origen etimológico se encuentra en la lengua griega y se refiere a algo formado por diversos componentes. Y es que así lo certifica su origen etimológico. En concreto, deriva del griego, exactamente de la suma de dos elementos como son el prefijo “poli-”, que es equivalente a “muchos”, y el sustantivo “meros”, que puede traducirse como “partes”.
La acepción más habitual del término hace mención a un compuesto, ya sea sintético, natural o químico, que se crea a través de un fenómeno conocido como polimerización, a partir de la repetición de unidades estructurales.

Puede decirse que los polímeros son macromoléculasque se forman con la vinculación de otras clases demoléculas denominadas monómeros. La síntesis de los polímeros se produce por una reacción provocada por sus monómeros que se denomina, como ya mencionábamos, polimerización.
La polimerización puede desarrollarse como una reacción en cadena o a través de diversos pasos o etapas.
los polímeros naturales son aquellos que están presentes en la naturaleza. En este grupo es posible incluir al ADN, las proteínas y la quitina, entre otros. Los polímeros sintéticos, en cambio, se producen de forma industrial mediante la manipulación de los monómeros. El poliéster, el PVC y el nailon son ejemplos de polímeros sintéticos.
 polímero natural:algodón
polímero natural:algodón
BORAX
El bórax(Na2B4O7·10H2O,borato de sodio o tetraborato de sodio) es un compuesto importante del boro. Es el nombre comercial de la sal de boro. Es un cristal blanco y suave que se disuelve fácilmente enagua; con densidad (decahidrato) de 1.73 g/cm3. Si se deja reposar al aire libre, pierde lentamente su hidratación y se convierte en tincalconita (Na2B4O7 •5 H2O). El bórax comercial generalmente se deshidrata en parte.
USOS
pesticidas
El bórax se utiliza ampliamente en detergentes, suavizantes, jabones, desinfectantes y pesticidas. Se utiliza en la fabricación de esmaltes, vidrio y cerámica. También se convierte fácilmente enácido bórico o en borato, que tienen muchos usos.

Como fundente
Una mezcla de cloruro de bórax y amonio se utiliza como fundente al soldar hierro y acero. Su función es bajar el punto de fusión del indeseado óxido de hierro.
En joyería
El bórax también se utiliza en joyería mezclado con agua como fundente al soldar oro, plata, etc. Permite que el metal fundido fluya uniformemente sobre el molde, y conserva el brillo y el pulido de la pieza a soldar. Ataca cierto tipo de piedras semipreciosas como toda la familia de las circonitas, las cuales se destruyen al contacto con el bórax y con una alta temperatura, necesaria para fundir el metal.
Heroína
Vidrios, pinturas y soldaduras
Se usa en la manufactura de vidrios, de componentes de pinturas, de soldaduras, de preservantede maderas.
También se usa como desoxidante y como ingrediente de abonos foliares.
Además se utiliza como aditivo en la aplicación de yesos, ya que reduce considerablemente el tiempo de fraguado del mismo.

Definición de polímeros - Qué es, Significado y Conceptohttp://definicion.de/polimeros/#ixzz41zWfacf5
https://www.google.com.mx/url?sa=t&rct=j&q=&esrc=s&source=web&cd=1&cad=rja&uact=8&ved=0ahUKEwjVgd62yKjLAhUMvIMKHW5sAVIQFggbMAA&url=https%3A%2F%2Fes.wikipedia.org%2Fwiki%2FB%25C3%25B3rax&usg=AFQjCNEiXyq3OtDPeI-fQx7d7zFASCDOnA&sig2=EeckI2glOaKTXM-XgB5svQ
MATERIAL:
-
2 vasos desechables.
-
2 cucharas desechables.
-
Plumón de aceite.
-
Guantes
SUSTANCIAS:
-
Pegamento blanco liquido.
-
Colorante vegetal líquido.
-
Borax.
-
Agua.
-
Acetona
-
Bicarbonato
PROCEDIMIENTO:
-
Rotula los vasos con los números 1 y 2.
-
En el vaso 1 vierte agua hasta la mitad y disuelve 1 cucharada de bórax.
-
En el vaso 2 vierte pegamento hasta una altura de 2 cm y agrega una cucharada de agua junto con 10 gotas de colorante y mezcla.
-
Vierte el contenido del vaso 1 en el vaso 2 y mezcla con movimientos envolventes; toma la sustancia entre tus manos y amasala hasta formar la pelota.
-
Sumerge la pelota en un poco de acetona, amásala nuevamente y registra tus observaciones
-
A esa misma pelota espolvoréale bicarbonato y observa que sucede
PROCEDIMIENTO EXPERIMENTAL
Primero rotulamos los vasos después agregamos el pegamento a uno de ellos y cada integrante del equipo realizo lo siguiente con diferentes cantidades y a ninguno nos dio un resultado exitoso por lo que seguimos intentando con diferentes cantidades sin tener éxito.
PROTOCOLO DE SEGURIDAD
Teníamos que tener mucho cuidado principalmente con el bórax y no jugar con los otros componentes pero no había mucho peligro.
OBSERVACIONES (IMÁGENES Y DESCRIPCIÓN):
Este es el ejemplo de un procedimiento

disolución de bórax en agua

Resistol con colorante

aquí se observa el Resistol, agua y colorante

Resultado de mezclar el contenido de los dos vasos

así es como quedo la mezcla (no funciono)
estos fueron nuestros mejores resultados aunque ninguno con el resultado deseado de que botara 20 cm mínimo
BORAX
AGUA
PEGAMENTO
COLORANTE
RESULTADO
1 cucharadita
Mitad del vaso
2 cm
0 gota
Funciono un poquito pero no del todo bien
½ de cuchara
1/3 del vaso
1 ½ cm
1 gota
No funciono
1/3 de cuchara
Mitad del vaso
1 cm
2 gotas
No funciono
2 cucharadas
¾ del vaso
½ cm
3 gotas
No funciono
1 ½ cucharadas
Mitad del vaso
2 cm
1 gotita
No se termino
2 cucharadas
¾ del vaso
2 cm
1 cucharita
Fue la que obtuvo mejores resultados
3 cucharadas
Mitad del vaso
3 cm
2 gotas
No funciono
ANÁLISIS:
-
¿Cuál es el efecto del bórax en el pegamento? El bórax diluido en el agua al ponerlo en el pegamento este absorbe el bórax que estaba en el agua y así generando una masa que es muy moldeable y que incluso puede llegar a botar (aquí esta presente un cambio químico y físico)
-
¿Cuál es la ecuación química que representa este cambio químico?
-
El borato de sodio forma un polímero entrecruzado
-CH2-CHOCOCH3-CH2- CHOCOCH3-CH2-CHOCOCH3(-(B(OH)4-)n
Seria un acetato de polivinil-boro.
El tetraborato de sodio NaB(OH)4 se disuelve en agua dando un ion Na+ y un ion tetraborato B(OH)4-.
CONCLUSIÓN:
Al elaborar la mezcla de bórax y agua y ponerla en el pegamento se observa que el pegamento reacciona al bórax y estos no se disuelven con el agua sino que forman una masa con el pegamento mientras el agua se queda en el vaso.
también se observo que es necesario encontrar un equilibrio entre el bórax, agua, pegamento y colorante (no es muy fácil) para poder obtener bien la pelota que fue la razón por la cual no nos funciono a nosotros pero si nos dimos cuenta que si es mucho bórax la mezcla se corta y si es poco se hace aguado.
También se usa como desoxidante y como ingrediente de abonos foliares.
Además se utiliza como aditivo en la aplicación de yesos, ya que reduce considerablemente el tiempo de fraguado del mismo.

Definición de polímeros - Qué es, Significado y Conceptohttp://definicion.de/polimeros/#ixzz41zWfacf5
https://www.google.com.mx/url?sa=t&rct=j&q=&esrc=s&source=web&cd=1&cad=rja&uact=8&ved=0ahUKEwjVgd62yKjLAhUMvIMKHW5sAVIQFggbMAA&url=https%3A%2F%2Fes.wikipedia.org%2Fwiki%2FB%25C3%25B3rax&usg=AFQjCNEiXyq3OtDPeI-fQx7d7zFASCDOnA&sig2=EeckI2glOaKTXM-XgB5svQ
MATERIAL:
- 2 vasos desechables.
- 2 cucharas desechables.
- Plumón de aceite.
- Guantes
SUSTANCIAS:
- Pegamento blanco liquido.
- Colorante vegetal líquido.
- Borax.
- Agua.
- Acetona
- Bicarbonato
PROCEDIMIENTO:
- Rotula los vasos con los números 1 y 2.
- En el vaso 1 vierte agua hasta la mitad y disuelve 1 cucharada de bórax.
- En el vaso 2 vierte pegamento hasta una altura de 2 cm y agrega una cucharada de agua junto con 10 gotas de colorante y mezcla.
- Vierte el contenido del vaso 1 en el vaso 2 y mezcla con movimientos envolventes; toma la sustancia entre tus manos y amasala hasta formar la pelota.
- Sumerge la pelota en un poco de acetona, amásala nuevamente y registra tus observaciones
- A esa misma pelota espolvoréale bicarbonato y observa que sucede
PROCEDIMIENTO EXPERIMENTAL
Primero rotulamos los vasos después agregamos el pegamento a uno de ellos y cada integrante del equipo realizo lo siguiente con diferentes cantidades y a ninguno nos dio un resultado exitoso por lo que seguimos intentando con diferentes cantidades sin tener éxito.
PROTOCOLO DE SEGURIDAD
Teníamos que tener mucho cuidado principalmente con el bórax y no jugar con los otros componentes pero no había mucho peligro.

disolución de bórax en agua

Resistol con colorante

aquí se observa el Resistol, agua y colorante

Resultado de mezclar el contenido de los dos vasos

así es como quedo la mezcla (no funciono)
ANÁLISIS:
CONCLUSIÓN:
Primero rotulamos los vasos después agregamos el pegamento a uno de ellos y cada integrante del equipo realizo lo siguiente con diferentes cantidades y a ninguno nos dio un resultado exitoso por lo que seguimos intentando con diferentes cantidades sin tener éxito.
PROTOCOLO DE SEGURIDAD
Teníamos que tener mucho cuidado principalmente con el bórax y no jugar con los otros componentes pero no había mucho peligro.
OBSERVACIONES (IMÁGENES Y DESCRIPCIÓN):
Este es el ejemplo de un procedimiento
Este es el ejemplo de un procedimiento

disolución de bórax en agua

Resistol con colorante

aquí se observa el Resistol, agua y colorante

Resultado de mezclar el contenido de los dos vasos

así es como quedo la mezcla (no funciono)
estos fueron nuestros mejores resultados aunque ninguno con el resultado deseado de que botara 20 cm mínimo
BORAX
|
AGUA
|
PEGAMENTO
|
COLORANTE
|
RESULTADO
|
1 cucharadita
|
Mitad del vaso
|
2 cm
|
0 gota
|
Funciono un poquito pero no del todo bien
|
½ de cuchara
|
1/3 del vaso
|
1 ½ cm
|
1 gota
|
No funciono
|
1/3 de cuchara
|
Mitad del vaso
|
1 cm
|
2 gotas
|
No funciono
|
2 cucharadas
|
¾ del vaso
|
½ cm
|
3 gotas
|
No funciono
|
1 ½ cucharadas
|
Mitad del vaso
|
2 cm
|
1 gotita
|
No se termino
|
2 cucharadas
|
¾ del vaso
|
2 cm
|
1 cucharita
|
Fue la que obtuvo mejores resultados
|
3 cucharadas
|
Mitad del vaso
|
3 cm
|
2 gotas
|
No funciono
|
- ¿Cuál es el efecto del bórax en el pegamento? El bórax diluido en el agua al ponerlo en el pegamento este absorbe el bórax que estaba en el agua y así generando una masa que es muy moldeable y que incluso puede llegar a botar (aquí esta presente un cambio químico y físico)
- ¿Cuál es la ecuación química que representa este cambio químico?
- El borato de sodio forma un polímero entrecruzado
-CH2-CHOCOCH3-CH2- CHOCOCH3-CH2-CHOCOCH3(-(B(OH)4-)n
Seria un acetato de polivinil-boro.
El tetraborato de sodio NaB(OH)4 se disuelve en agua dando un ion Na+ y un ion tetraborato B(OH)4-.
también se observo que es necesario encontrar un equilibrio entre el bórax, agua, pegamento y colorante (no es muy fácil) para poder obtener bien la pelota que fue la razón por la cual no nos funciono a nosotros pero si nos dimos cuenta que si es mucho bórax la mezcla se corta y si es poco se hace aguado.